Chemwizard
Τιμώμενο Μέλος


Σπάω την ερώτηση σου σε κομμάτια:Έχετε δίκιο, θα προσπαθήσω να είμαι πιο σαφής.
Έχω μπερδευτεί με τη σειρά δραστικότητας στις αντιδράσεις απλής αντικατάστασης. Τι γίνεται όταν ένα μέταλλο ή αμέταλλο είναι δραστικότερο από κάποιο άλλο;
Σας ευχαριστώ!
Τι είναι ένα μέταλλο;
Τι είναι ένα αμέταλλο;
Τι κάνει ενα μέταλλο, πιο δραστικό από ένα άλλο;
Τι κάνει ένα αμέταλλο πιο δραστικό από ένα άλλο;
Πώς τα συγκρίνεις;
Τι θα συμβεί μεταξύ τους;
Ποιο το είδος αντίδρασης;
Chemwizard
Τιμώμενο Μέλος


Kαλησπέρα.Κατάλαβα. Θα μπορούσατε μήπως να μου εξηγήσετε αυτό με τη δραστικότητα; Σας ευχαριστώ
Δραστηριότητα τίνος, και όσον αφορά τι;
Γενικα, το ιδανικό είναι η ερώτηση να είναι σαφώς διατυπωμενη, αφενός διότι αυτό δείχνει πως έχουμε κατανοήσει το προβλημα μας, αφετέρου δε, αυξάνει τις πιθανότητες να έχουμε σαφή απάντηση.
Chemwizard
Τιμώμενο Μέλος


Μπορεί να είναι ενεργειακοί με βάση την ενθαλπία, η την ενέργεια κατά Gibbs, μπορεί να είναι οξειδωαναγωγικές ή οξεοβασικές αντιδράσεις, στην οργανική δε υπάρχουν διάφοροι μηχανισμοί, ανάλογα πχ αν έχουμε ηλεκκτρονιόφιλη ή πυρηνοφιλη προσθήκη ή αντικατάσταση, κτλ κτλ.Οι βασικοί κανόνες ας πούμε. Οτιδήποτε θεωρείτε πως θα με βοηθήσει να τα ξεκαθαρίσω.
Chemwizard
Τιμώμενο Μέλος


Chemwizard
Τιμώμενο Μέλος


Παιδιά στον αριθμό οξείδωσης πρέπει να μάθω απέξω τους αριθμούς της οξειδώσης των χημικών στοιχειων; ευχαριστώ
Ξεκιμαμε από τα βασικα:
-Τι ορίζουμε οξείδωση και τη αναγωγή; (υπάρχουν τρεις τρόποι να οριστούν, ο τρίτος εμπλέκει τον αριθμό οξείδωσης)
-Γίνεται να υπάρχει το ενα χωρίς το άλλο;
-Τι ορίζουμε αριθμό οξείδωσης; (δυο περιπτώσεις, μια σε ενα αλας, μια σε μια οποιοπολική ένωση;
(Υπενθυμιση: τι ορίζουμε ως ηλεκτραρνητικοτητα; τι ρολο παιζει εδω; )
-Ολα τα στοιχεία έχουν παντα εναν Α.Ο.; (spoiler alert, όχι)
-Πως βρίσκω αυτά που δεν εχουν μονο εναν, σε ενα φορτισμένο ή μη μόριο; (Χρησιμοποιωντας αυτα που έχουν μόνο εναν, άρα αυτα τα μαθαίνεις)
*Βonus ερωτηση: Τι παιζει με τα στοιχεια μεταπτωσης κι έχουν διαφορους Α.Ο;
Chemwizard
Τιμώμενο Μέλος


Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


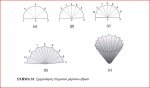
Μιας και βρισκόμαστε σε φάση εργαστηρίων...έχουμε ως επόμενο θέμα τη διήθηση. Έχω ως απορία, ποια είναι η ουσιαστική διαφορά πτυχωτού ηθμού με ηθμό σε σχήμα κώνου? Ίσως έτσι καταφέρω να συμπεράνω πότε χρησιμοποιούμε τον ένα και πότε τον άλλο. (Σημ. όταν μιλάμε για διήθηση, εννοούμε το διαχωρισμό στερεού-υγρού σε ετερογενές μείγμα)

Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Συνημμένα
Chemwizard
Τιμώμενο Μέλος



Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


ναι τον φωσφορο εννοω απλα ξεχασα να το γραψω
Οπως είπα η ένωση συνολικα,επειδη είναι ουδετερη,πρέπει να έχει 0.Καθε οξυγόνο έχει -2,ενώ κάθε υδρογόνο έχει +1.
Αρα +1 Χ 3 + Ρ Χ 1 + ( -2) Χ 4 = 0.
Αρα Ρ = 5.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


μπορει να μου πει καποιος τον αριθμο οξειδωσης του Η3PO4?
Ενώσεις που δεν έχουν φορτιο εχουν Α.Ο 0.Μήπως εννοείς πόσο έχει ο φωσφόρος εκεί?
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Η εφαρμοφή λεει:
Ποσο ζυγίζει 1 άτομο υδρογονο αν Ar H = 1
Παντως ευχαριστω για τον τυπο
1 mol αγόρι μου ζυγίζει ένα γραμμάριο (παντα ενα μολ ζυγίζει οσο το Ar ή το Mr ) και περιέχει 6,02 επί 10 εις την 23 ατομα.Διαιρεσε λοιπον το ένα γραμμάριο με τα τοσα ατομα,να δεις πόσο ζυγίζει το ενα ατομο.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος



(Εσύ βοηθάς τον εαυτό σου όταν ψάχνεσαι)
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Ααααα...Ναι...αλλα να σε ρωτησω και κατι ακομα...ας πουμε στο μονοξειδιο του ανθρακα και στο τριοξειδιο του θειου το ιδιο γινετα???
Προσεξε,αν εχεις θειικο οξυ,H2CO3,αν του βγαλεις ενα νερο παιρνεις το CO2,ενω αν δεις τον Α.Ο. του C στο θειικο οξυ,αυτος είναι +4.Αν εσυ βαλεις στον C δυο οξυγονα που καθενα εχει -2 κανεις το CO2.
Ο ανθρακας ομως μπορει να εχει και Α.Ο. +2,οποτε τοτε σχηματιζει το CO.
Καταλαβαμε?

Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Αχα...Νομιζω το καταλαβα...δηλαδη για να το βρω 8α παιρνω το οξυ,8α βρισκω τον Α.Ο και μετα 8α τα πηγαινω χιαστι ετσι?
Αριθμος οξειδωσης ειναι στο μεταλλο τα ηλεκτρονια που δινει,ενω στο αμεταλλο αυτα που παιρνει (χονδρικα μιλώντας)Αυτα τα φορτια πρεπει σε μια ενωση μεσα να αλληλοεξουδετερωνονται,ωστε η ενωση αν δεν ειναι φορτισμενη,να εχει φορτιο 0.Οποτε αν ο φωσφορος σου εχει Α.Ο. 5 ,κι το οξυγονο εχει -2 εσυ τι κανεις.Θελεις απο τη μια να εχεις τοσους φωσφορους,κι απο την αλλη τοσα οξυγονα,ωστε να εχεις δυο τετοια φορτια που να ειναι αντιθετα,για να σου βγαζει στην ενωση 0.Αν παρεις 2 φωσφορους (5 ο ενας) και 5 οξυγονα (-2 το ενα)εχεις 2Χ5 =10 για φωσφορο,και 5 Χ -2 = -10 για τα οξυγονα,αρα οσα ηλεκτρονια δωσαν τα μεταλλα,τοσα πηραν τα αμεταλλα,αρα εχουμε εξουδετερωση φορτιων,και η ενωση P2O5 εχει συνολικο φορτιο 0.Καταλαβες τωρα γιατι τα βαζεις χιαστι?
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Οξειδια λεει το βιβλιο της Α,σελίδες 92 και 93 (ανοιξε μαζί μου),είναι οι ενώσεις στοιχείων (είτε μέταλλο είτε αμέταλλο),με οξυγόνο.(Το οποιο επισης στοιχειο είναι,αλλα αυτες οι ενωσεις ολο και καποιο ενδιαφερον θα έχουν,οπότε τις μελετάμε)
Τα οξειδια σου λεει,συνηθως ειναι ενωσεις που εχουν τυπο Σ2Οχ. Οπου Σ,βάζεις ένα Μεταλλο (Να,Κ,Fe,κλπ),ή ενα Αμεταλλο (Ν,S,C)
Οπου χ βάζεις έναν αριθμό.
Καθε ενωση αυτης της μορφης θα πρεπει να την αναγνωριζεις ως "Οξειδιο του Σ"
Δηλαδη το CO2 πχ ειναι "Διοξειδιο του ανθρακα",το δι- μπαινει λογω του αριθμου 2.
Για να βρεις το πως βγαίνει ενα ΟΞΙΝΟ ΟΞΕΙΔΙΟ:
(οξινα οξειδια ειναι αυτα που παιρνεις ενα οξυ,και τους βγάζεις ενα νερο.Συνηθως εχουν αμεταλλο μαζι με Ο,το γιατι είναι άλλη ιστορία)
θεωρητικα γινεται αυτο.
Απο ανθρακικο οξυ πχ,αν αφαιρεσεις H20 παιρνεις το οξειδιο CO2,και το διοξείδιο είναι ενα οξειδιο,το λεει το ονομα του καλη μου.Απλά ο C σχηματίζει εκτος απο αυτό κι αλλα ,πχ CO (μονοξειδιο)
Αυτό ομως δε μπορεις να το κανεις παντα.Τοτε κανεις το εξης.Παρε το Η3PO4.Βρες αριθμο οξειδωσης του P.Aν ξερεις να τον βρεις,ειναι +5.
Τοσος πρεπει να ειναι και στην ενωση που προκυπτει,αυτη που ψαχνεις,και θα ειναι οξειδιο.Τι κανεις Λοιπον.Εχεις μια ενωση PxOψ.(ορισμος ειπαμε,λεει πως κατι αυτης της μορφης ειναι οξειδιο)To οξυγονο θα εχει παντα -2,και το P εδω θα εχει +5.Αντιστρεφοντας τους αριθμους,ωστε αν πολλαπλασιασεις τον αριθμο ενος στοιχειου με την απολυτη τιμη του Α.Ο του αλλου τα δυο γινομενα να ισουνται,σου βγαινει πως το οξειδιο που θελεις ειναι P2O5.
Με πιανεις?
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Πώς μπορούμε να βρούμε τον αριθμό οξείδωσης?Δηλαδή ποία εξίσωση ακολουθούμε και πως προκύπτει αυτή?
Δε χρειάζεται να κάνεις πράξεις η κατι τέτοιο.
Αν μιλαμε για το ενα ακρο,τις ιοντικες ενωσεις,που εχουμε κλεψιμο ηλεκτρονιων,ισχυει το εξης απλο.Οσα ηλεκτρονια κλεψεις απο τον αλλο,τοσο - αριθμο οξειδωσης εχεις.Κι εκεινος αποκτα αντιστοιχα τοσο + αριθμο οξειδωσης.Πχ στο ΝαCl,το Να που στην εξωτερικη του στιβαδα εχει ενα ηλεκτρονιο μοναχο του,το δινει στο Cl που εχει ηδη 7.Το Cl εχει -1 και το Να +1.Αυτο το "κλεψιμο"γινεται γιατι ολα τα στοιχεια θελουν να εχουν οχτω ηλεκτονια στην εξωτερικη τους στιβαδα,ειναι πιο σταθερα ετσι.Με αυτο τον τροπο και το χλωριο εχει 8,και το νατριο μενει με την οχταδα της παρακατω στιβαδας.Ιοντικες ενωσεις κανουν μεταλλα.Ουσιες δηλαδη αριστερα στον περιοδικο πινακα,που εχουν πολυ λιγα ηλεκτρονια αρα δεν παιζει να συμπληρωσουν την τελευταια στιβαδα.
Η ενδιαμεση κατασταση ειναι οι πολικες ομοιοπολικες ενωσεις.Πρέπει να κατανοήσεις κατ'αρχήν γιατι τα στοιχεία έχουν την τάση να ενώνονται με άλλα στοιχεία.Οπως ειπα σε ενα φιλο στη Β Λυκειου πριν λίγο,αυτο γινεται γιατι κάθε στοιχείο θέλει να μοιράζεται με αλλα στοιχεία ηλεκτρόνια,ωστε να νιώθει το καθενα 8 γυρω του.(Η δυο αν μιλαμε για το Η)Καθε δεσμος ειναι μοιρασμα ενος ηλεκτρονιου απο καθε ατομο,αρα συνολο δυο.Καθε ηλεκτρονιο που μοιραζεται το νιωθουν και τα δυο.Ομως μοιραζονται εξιου τα ηλεκτρονια απο τα ατομα?Στις πολικες ομοιοπολικες οχι ,οσο πιο πολλα ατομα εχει ηδη ενα στοιχειο πανω του (απο 1 ως 7,αυτα που εχουν ηδη 8 δεν αντιδρουν)τοσο πιο ευκολα τραβα ολα τα ηλεκτρονια πάνω του.ΤΟΣΟ ΠΙΟ ΗΛΕΚΤΡΑΡΝΗΤΙΚΟ ΕΙΝΑΙ.Αριθμος οξειδωσης μια ομοιοπολικης ενωσης,ειναι μια πειραματικη ποσοτητα(δεν υπαρχει δηλαδη στην πραγματικοτητα)το "φορτιο" που προκυπτει αν,ολα τα ΚΟΙΝΑ ηλεκτρονια ζευγη ηλεκτρονιων(ολοι οι δεσμοι,δωθουν πανω στο πιο ηλεκτραρνητικο ατομο.πχ στην ενωση CH3OH,o ανθρακας ενωνεται με τα λιγοτερο ηλεκτραρνητικα του Η,και το περισσοτερο ηλεκτραρνητικο του Ο.Με τα πρωτα μοιραζεται απο ενα ηλεκτρονιο,και με το δευτερο παλι αλλο ενα.Αρα τα Η εχουν αριθμο οξειδωσης +1,ο ανθρακας -1Χ3 +2 (επειδη το οξυγονο ειναι ηλεκτραρνητικοτερο)=-1,και το οξυγονο -2,ενα για καθε ηλεκτρονιο που μοιραζεται.Αν τα προσθεσουμε ολα μαζι ειναι 3Χ+1 +(-2)+(-2)+1=0.μηδεν πρεπει να βγαινει η ενωση συνολικα,γιατι δεν ειναι φορτισμενη αλλα ουδετερη.Αλλιως συνολικα πρεπει να μας βγαινει το φορτιο της ενωσης)
Το αλλο ακρο ειναι η μη πολικες ενωσεις,εκει που τα ατομα ειναι ιδια,πχ Ο2.δεν εχουμε ουτε κλεψιμο,ουτε μοιρασμα περισσοτερο στο ενα παρα στο αλλο(οπως στις ομοιοπολικες πολικες)αρα δεν εχουμε και φορτιο,αρα ουτε και αριθμο οξειδωσης,αρα το καθε Ο εχει αριθμο οξειδωσης Ο.
Ομοιοπολικες ενωσεις,(πολικες η μη πολικες)κανουν ατομα που δεν εχουν τοση διαφορα ηλεκτραρνητικοτητας,ωστε να μποροει να κλεψει ηλεκτρονια το ενα στοιχειο απο καποιο αλλο στοιχειο.
Το καταλαβαμε Μαρια?

Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Χρυσάνθη μου τα μπερδεψες λιγο.Διασταση ενος οξεος ή μιας βάσης στο νερο,ειναι το ΣΠΑΣΙΜΟ της με απλα ελληνικά.Χμ,δηλαδη για παραδειγμα αν βάλω μέσα σε νερο HCl,αυτα γινονται H και Cl οπως ηταν πριν ενωθουν ακριβώς?Η απαντηση ειναι οχι,κι η δικαιολογιση ευκολη. :Ενα Η κ ενα Cl για να ενωθουν συνεισφερουν απο ενα ηλεκτρονιο.Τι μας λεει η θεωρια για τον ομοιοπολικό δεσμό?Οτι ενα ζευγος ηλεκτρονιων ελκεται απο το πιο ηλεκτραρνητικο ατομο απο τα δυο.Δηλαδη ενα ζευγαρακι ηλεκτρονιων που μοιραζονται το Η και το Cl για να ενωθουν,ελκεται πιο πολυ απο το Cl.Οταν δηλαδη η ενωση παει να υποστει στο νερο διασταση,να σπασει δηλαδη,το Cl στο παραδειγμα μου,ή το CN(ενωση ανθρακα νατριου,αλλιως κυανιο)που ειναι πιο ηλεκτραρνητικα απο το Η κραταei και τα δυο μοιρασμενα ηλεκτρονια για παρτη του,ετσι έχουμε κατα τη διασταση CN-(αρνητικά φορτισμένο) και Η+ αυτο είναι η διασταση,δηλαδη το ΗCN παθαινει διασταση οχι τα προιοντα αυτης!ΜΕρικα οξεα ομως ειναι ισχυρα και μερικα οχι.Τι σημαινει αυτο?Αν εχεις ενα μπουκαλακι με 10 μορια ισχυρου οξεος,θα δεις οτι και τα 10 παθαινουν διασταση,δηλαδη σπανε,ενω αν εχεις ενα μπουκαλακι με 10 μορια ασθενους,τα περισσοτερα (πχ 8,δε σπανε καν,αλλα το κανουν μονο πχ τα 2),ετσι το ΗCN,που ειναι ασθενες,διισταται σε ενα μικρο μερος του,δηλαδη τα περισσοτερα απο το συνολο των μοριων δεν διιστανται μεσα στο νερο!ποιο μερος του HCN δεν παθαινει διασταση? το CN?
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Aν μου εξηγησεις το προβλημα σου αναλυτικα...Eντάξει αυτό με το θείο το ξεκαθάρισα. Μπορεί να μου λύσει κάποιος την άλλη απορία που δεν θα κοιμηθώ αν δεν το βρω!
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Είναι ιον που προκυπτει οταν βαλεις θειικο οξυ Η2ΣΟ3σε νερο.φευγουν δυο πυρηνες υδρογονου(θετκο φορτιο αφου δεν παιρνουν και τα ηλεκτρονια μαζι) αλλα τα ηλεκτραρνητικα θειο και οξυγονο κρατανε τα κοινα ηλεκτρονια, αρα μενει κατι με -2 φορτιο.Αριθμος οξείδωσης θειικου ιοντος = 3Χ-2 +4(θειο)=-2.Ποιος ειπε οτι το θείο εχει παντα +6?ΜΟΝΟ ΜΕΡΙΚΑ ΣΤΟΙΧΕΙΑ ΕΧΟΥΝ ΣΤΑΘΕΡΟ.ΑΝ ΕΙΧΑΝ ΟΛΑ Η ΟΞΕΙΔΟΑΝΑΓΩΓΗ ΔΕ ΘΑ ΕΙΧΕ ΝΟΗΜΑ.το μαγγανιο εχει 6 διαφορετικους αριθμους πχ.Το θειο συνηθως εχει -2 οπως το οξυγονο.Όχι δεν λέω αυτό. Επειδή υπάρχει τρόπος στο βιβλίο σχετικά με το πως βρίσκω τον Α.Ο εγώ δεν ξέρω αν το ΣΟ3 είναι ένωση ή ιόν. Ο Νίκος λέει ότι είναι από τη μία ιόν αλλά μετά λέει ότι είναι Σ=6. Αλλά αυτός τώρα είναι άφαντος. Κάτσε να απαντήσει και μετά να δω αν θα χω πάλι την απορία..
.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


ΤΟ SO3 εχει αριθμο οξείδωσης -2 (το θειικο οξυ Η2ΣΟ3 εχει 0)Την αλλη απορια δεν την καταλαβαΛοιπόν όπως μάλλον θα καταλάβετε γράφω Παρασκευή Χημεία. Επιτέλους μέχρι τώρα σχεδόν τελείωσα την ύλη. Η βασική μου απορία είναι η εξής:
σελ131 βιβλίου. Ρωτά πόσο ζυγίζει το 1 άτομο υδρογόνου. Γιατί διαιρεί στην λύση με 1,66*10 στην -24 και όχι με το ΝΑ που είναι 6,02*10 στην 23;
Επίσης μια άλλη απορία μου σχετικά με τον Α.Ο. του SO3. To παίρνω σαν ρίζα ή κανονικά σαν ένωση για να το βγάλω; Απ ότι κατάλαβα το παίρνω σαν ένωση γιατί το θείο θα χει στάνταρ Α.Ο με βάση το πινακάκι της σελ του μαθήματος. Αν το πάρω σαν ρίζα βγαίνει 5. Αλλά το θειώδες πάντα με προβλημάτιζε γιατί για να λέγεται θειώδες δεν είναι το προηγούμενό του το θειικό που είναι ρίζα με -1; Τι είναι βρε παιδιά γιατί πολύ με ζωρίζει αυτό το θειώδες. Το ξέρω ότι λέγεται και τριοξείδιο του θείου, αλλά μπορεί κανείς να απαντήσει, αν είναι ρίζα ή απλή ένωση;
ΤΟ SO3 εχει αριθμο οξείδωσης -2 (το θειικο οξυ Η2ΣΟ3 εχει 0)
Νίκο αν είσαι μέσα πλιζ απάντησε. Δεν παρακαλώ θεούς άλλο πλέον, αφού είναι γνωστό πως είσαι ο διάδοχος του πυρηνικού φυσικού!!!!!!!!!!!!!!!!!!
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Η αλήθεια είναι πως μπερδεύτηκα.
Σ'ευχαριστώ πάντως για την απάντηση σου. Αυτό που δεν μπορώ να καταλάβω είναι γιατί μερικές φορές κάποια στοιχεία προσλαμβάνουν/δίνουν περισσότερα e- απ'ότι τους χρειάζονται. Δηλαδή για παράδειγμα ο σίδηρος δεν θέλει 2 για να συμπληρωθεί η εξωτερική του στιβάδα; Γιατί μερικές φορές έχει Α.Ο. +3;
Καταλαβαίνω ότι σε κάποιες εξισώσεις αλλάζει ο Α.Ο. αλλά αυτό που δεν καταλαβαίνω είναι γιατί γίνεται αυτό. Προσπαθώ να το οπτικοποιήσω στο μυαλό μου σκεφτόμενος το άτομο του κάθε στοιχείου να δίνει και να παίρνει e-. Αλλά για παράδειγμα με το Θείο, νόμιζα ότι κάνει ομοιοπολικό δεσμό για να συμπληρωθεί η εξ. στιβάδα του.
Κατ'αρχας για να συμπληρώσει την εξώτατη στιβάδα χρειάζετα 4 e-(έχει 6 και χωράει 10,αυτό διδάσκεται αναλυτικά στη Γ λυκείου.Με αυτο το σκεπτικό λοιπον,σύμφωνα με ό,τι σου είπε η καθηγήτρια την οποία κι εγώ ευχαριστώ,περιμένω να αποβάλλει το πολύ 6 και να προσλαμβάνει το πολύ 4.ισώς όμως τα ηλεκτρόνια 4s να κάνουν κουμμάντο.Δυστυχώς είμαι πρωτοετής και δεν το έχω μελετήσει ακόμη.
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


NaHCO3 + HI ---> NaI + H2O + CO2
Ba(NO3)2 + Na2SO4 ---> BaSO4 + 2NaNO3
BaCO3 + 2HCl ---> BaCl2 + H2O + CO2

στις λεγόμενες αντιδράσεις καταβύθισης,το αν θα γινει η αντιδραση η οχι εξαρτάται απο τον εξης παράγοντα:από ευδιαλυτα προιόντα (aq) πρέπει να οδηγούμαστε σε ενα στερεό (s).άλλη πιθανότητα πραγματοποίησης της αντίδρασης είναι η δημιουργία αερίου.διαφορετικα τα αντιδρώντα μενουν ως εχουν.Οποιος θέλει την πλήρη εξηγηση του τι συμβαίνει,γιατί συμβαίνει,και μια φωτοτυπία με το ποιά προιόντα ειναι στερεα και ποια όχι,μπορεί να με προσθέσει στο msn:gianniskeeper@hotmail.com ,στέλνοντας μου μηνυμα ποιος είναι και το λογο που με προσεθεσε.
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Έχω msn (φυσικά....) αλλά δε το δίνω σε δημόσια φόρα....
μπορειτε να το στειλετε στο παιδι σε ιδιωτικο μηνυμα,αν θελετε φυσικα.
Σημείωση: Το μήνυμα αυτό γράφτηκε 15 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
-
Το forum μας χρησιμοποιεί cookies για να βελτιστοποιήσει την εμπειρία σας.
Συνεχίζοντας την περιήγησή σας, συναινείτε στη χρήση cookies στον περιηγητή σας.
 Αρχική Forum
Αρχική Forum
 Ρωτήστε κάτι
Ρωτήστε κάτι
 Προσωπικές Συζητήσεις
Προσωπικές Συζητήσεις
 Πανελλαδικές
Πανελλαδικές
 Αγγελίες
Αγγελίες
 Συνδεδεμένοι Χρήστες
Συνδεδεμένοι Χρήστες
 Λίστα Αποκλεισμένων
Λίστα Αποκλεισμένων
 Υπεύθυνοι του Forum
Υπεύθυνοι του Forum
 e-steki
e-steki